ЁвУДиХЪСЁвУУеДЭЁЋь (Balancing Redox Equation)
ЁвУДиХЪСЁвУУеДЭЁЋь (Balancing Redox Equation)
ЁвУДиХЪСЁвУУеДЭЁЋьСеЄЧвСТишЇТвЁсХаЋбКЋщЭЙЁЧшвЁвУДиХЪСЁвУЂЭЇЛЏдЁдУдТвИУУСДв ЛЏдЁдУдТвУеДЭЁЋьКвЇЛЏдЁдУдТвЭЙиРвЄЗбщЇЫСДрЁешТЧЂщЭЇЁбКЁвУрЁдДЛЏдЁдУдТвУеДЭЁЋьХщЧЙ ц рЊшЙ
H2 + Cl2 → 2HCl уЙЂГаЗешКвЇЛЏдЁдУдТвЈаСеЗбщЇЭЙиРвЄЗшерЁешТЧЂщЭЇЁбКЁвУрЁдДЛЏдЁдУдТвУеДЭЁЋь уЙЂГаЗшеЭЙиРвЄЭеЁЪшЧЙЫЙшжЇрЁдДЛЏдЁдУдТвИУУСДв рЊшЙ
KMnO4 + NaCl + H2SO4 → Cl2 + K2SO4 + MnSO4 + H2O + Na2SO4
- ЪшЧЙЗешрЁдДЛЏдЁдУдТвУеДЭЁЋьЄзЭИвЕиЗешСеЁвУрЛХешТЙсЛХЇрХЂЭЭЁЋдрДЊбЙ фДщсЁш Mn уЙ KMnO4 сХа Cl уЙ NaCl
- ЪшЧЙЗешрЁдДЛЏдЁдУдТвИУУСДвЄзЭИвЕиЗешфСшрЛХешТЙсЛХЇрХЂЭЭЁЋдрДЊбЙ фДщсЁш K O Na H сХа S
ЁвУДиХЛЏдЁдУдТвУеДЭЁЋьЗешСеЛЏдЁдУдТвИУУСДвУЧСЭТйшДщЧТ уЫщДиХЪшЧЙЗешрЁдДЛЏдЁдУдТвУеДЭЁЋьЁшЭЙ сХщЧЈжЇДиХЪшЧЙЗешрЁдДЛЏдЁдУдТвИУУСДв ЙЭЁЈвЁЙбщЙсХщЧТбЇрЁешТЧЂщЭЇЁбКРвЧасЧДХщЭСЂЭЇЛЏдЁдУдТвЧшврЛчЙЁХвЇЫУзЭрЛчЙЁУДЫУзЭрЛчЙрКЪЭеЁДщЧТ ЁвУДиХЪСЁвУУеДЭЁЋьЭвЈЗгфДщ 2 ЧдИеЄзЭ
1. ДиХЪСЁвУУеДЭЁЋьтДТуЊщрХЂЭЭЁЋдрДЊбЙ (Balancing redox equation using oxidation number)
2. ДиХЪСЁвУУеДЭЁЋьтДТуЊщЛЏдЁдУдТвЄУжшЇрЋХХь (Balancing redox equation using half reaction)
ЁвУДиХЪСЁвУУеДЭЁЋьтДТуЊщрХЂЭЭЁЋдрДЊбЙ СеЂбщЙЕЭЙЪгЄбДбЇЙещ
1. ЫвЕбЧУеДдЧЋь (ИвЕиЗешСерХЂЭЭЁДЋдрДЊбшЙрОдшСЂжщЙ) сХаЕбЧЭЭЁЋдфДЋь (ИвЕиЗешСерХЂЭЭЁЋдрДЊбЙХДХЇ) рХЂЭЭЁЋдрДЊбЙЗешрОдшСЂжщЙЫСвТЖжЇЈгЙЧЙЭдрХчЁЕУЭЙЗешЕбЧУеДдЧЋьЛХшЭТЭЭЁфЛ рХЂЭЭЁЋдрДЊбЙЗешХДХЇЫСвТЖжЇЈгЙЧЙЭдрХчЁЕУЭЙЗешЕбЧЭЭЁЋдфДЋьУбКфЧщ рЊшЙ
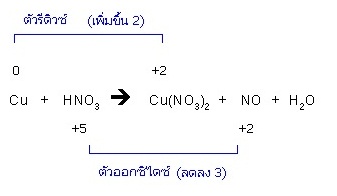
2. ЖщврХЂЭЭЁЋдрДЊбЙЗешрОдшСЂжщЙСеЄшврЗшвЁбКрХЂЭЭЁЋдрДЊбЙЗешХДХЇ сЪДЇЧшвЈгЙЧЙЭдрХчЁЕУЭЙЗешЕбЧУеДдЧЋьЛХшЭТЭЭЁфЛ ЁбКЈгЙЧЙЭдрХчЁЕУЭЙЗешЕбЧЭЭЁЋдфДЋьУбКрЭвфЧщСеЈгЙЧЙрЗшвЁбЙ уЫщДиХЪСЁвУЕшЭфЛЈЙЈК сЕшЖщврХЂЭЭЁЋдрДЊбЙЗешрОдшСЂжщЙсХаХДХЇСеЄшвфСшрЗшвЁбЙ уЫщЫвЕбЧрХЂЗешрЫСваЪССвЄйГрХЂЭЭЁЋдрДЊбЙЗешрОдшСсХаХДрОзшЭуЫщфДщЄшврЗшвЁбЙ сХщЧуЫщуЊщЕбЧрХЂЗешЙгСврЛчЙЕбЧЄйГЙбщЙ рЛчЙЈгЙЧЙтСХ ЂЭЇЕбЧУеДдЧЋьЫУзЭЕбЧЭЭЁЋдфДЋьЕвСХгДбК
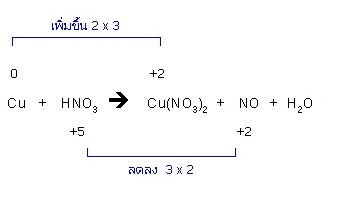
3. ДиХЈгЙЧЙтСХЂЭЇЕбЧУеДдЧЋьЁбКМХдЕРбГБьЗешрЁдДЈвЁЕбЧУеДдЧЋьуЫщрЗшвЁбЙ сХаДиХЈгЙЧЙтСХ ЂЭЇЕбЧЭЭЁЋдфДЋьЁбКМХдЕРбГБьЗешрЁдДЈвЁЕбЧЭЭЁЋдфДЋьуЫщрЗшвЁбЙДщЧТ
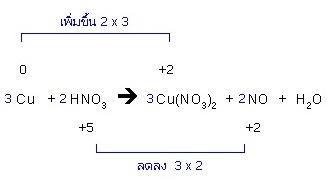
4. ЖщвСеЁУДЭТйшуЙЛЏдЁдУдТвуЫщОдЈвУГвДбЇЙещ (ЕбЧЭТшвЇЙещрЛчЙсКК 4.2)
4.1 ЁУДфСшрЁдДЛЏдЁдУдТвУеДЭЁЋь ЪбЇрЁЕфЭЭЭЙХКЂЭЇЁУД(ЄйшрКЪ)фСшрЛХешТЙУйЛфЛрЛчЙЭТшвЇЭзшЙ ЁУГеЙещДиХЪСЁвУтДТЁвУЗгуЫщЈгЙЧЙтСХЂЭЇЁУДЗвЇЪвУЕбщЇЕщЙ уЫщСеЈгЙЧЙтСХрЗшвЁбКЈгЙЧЙтСХЂЭЇфЭЭЭЙХКЂЭЇЁУД(ЄйшрКЪ)ЗбщЇЫСДЗвЇДщвЙМХдЕРбГБь ЗешЭвЈЭТйшуЙМХдЕРбГБьЊЙдДрДеТЧЫУзЭЫХвТЊЙдДЁчфДщ
4.2 ЁУДрЁдДЛЏдЁдУдТвУеДЭЁЋьКвЇЪшЧЙ ЪбЇрЁЕЈвЁфЭЭЭЙХКЂЭЇЁУДСеЁвУрЛХешТЙУйЛфЛрЛчЙЪвУуЫСшКвЇЪшЧЙ сЕшТбЇЄЇСефЭЭЭЙХКуЙУйЛрДдСрЫХзЭЭТйшДщЧТ уЙЁУГеЙещуЫщЕУЧЈЪЭКДйЧшвфЭЭЭЙХКЂЭЇЁУДЗешЭТйшуЙУйЛрДдСЗвЇДщвЙМХдЕРбГБьТбЇСеЭТйшЁештСХ уЫщрОдшСЈгЙЧЙтСХЂЭЇЁУДЗвЇЪвУЕбщЇЕщЙЭеЁрЗшвЙбщЙ ЕбЧЭТшвЇТещСеЁУД HNO3 ЭТйшуЙЛЏдЁдУдТв ЄйшрКЪЂЭЇСбЙЄзЭ NO3- ЈарЫчЙфДщЧшвСеЭТйшуЙМХдЕРбГБь 6 тСХ ЈжЇЕщЭЇрОдшЭС HNO3
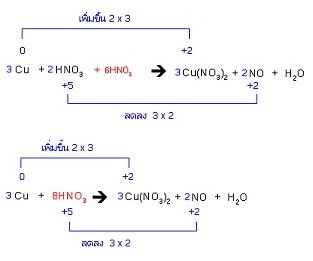
4.3 ЁУДрЁдДЛЏдЁдУдТвУеДЭЁЋьЗбщЇЫСД ЪбЇрЁЕЈвЁфСшСефЭЭЭЙХКЂЭЇЁУДуЙУйЛрДдСрЫХзЭЭТйшрХТуЙМХдЕРбГБь ЁУГеЙещуЫщДиХЪСЁвУЕшЭфЛтДТфСшЕщЭЇрОдшСЈгЙЧЙтСХЂЭЇЁУДЗвЇЪвУЕбщЇЕщЙ
5. ДиХЪСЁвУЪшЧЙЗешфСшрЁдДЛЏдЁдУдТвУеДЭЁЋь сХщЧЗгуЫщрЛчЙЭбЕУвЪшЧЙЭТшвЇЕшгрЗшвЗешЈаЗгфДщ
6. ЖщвЛЏдЁдУдТврЁдДЂжщЙуЙЪвУХаХвТЁУДКвЇЄУбщЇЈаОКЧшвЫХбЇЈвЁДиХЪСЁвУЗиЁЪшЧЙсХщЧ ТбЇЂвДЭаЕЭСЂЭЇ H ЫУзЭ O ЗвЇДщвЙуДДщвЙЫЙжшЇ уЫщсЁщЛбЫвДбЇЙещ
6.1 ДщвЙуДЂвД H уЫщрЕдС H+ ЕвСЈгЙЧЙЗешЂвД
6.2 ДщвЙуДЂвД O уЫщрЕдС H2O ЕвСЈгЙЧЙтСХЗешЂвД ДбЇЕбЧЭТшвЇ (ЕбЧЭТшвЇуЫСш)
ЗвЇЋщвТСе O = 4 ЗвЇЂЧвТбЇфСшСе ЕщЭЇрЕдС 4H2O сЕшЁчСеМХуЫщЗвЇЂЧвСе H = 8 ЂГаЗешЗвЇЋщвТТбЇфСшСе ЕщЭЇрЕдС 8H+ ЗвЇЋщвТ
7. ЖщвЛЏдЁдУдТврЁдДЂжщЙуЙЪвУХаХвТрКЪКвЇЄУбщЇЈаОКЧшвЫХбЇЈвЁДиХЪСЁвУЗиЁЪшЧЙсХщЧ ТбЇЂвДЭаЕЭСЂЭЇ H ЫУзЭ O ЗвЇДщвЙуДДщвЙЫЙжшЇ уЫщсЁщЛбЫвДбЇЙещ
7.1 ДщвЙуДЂвД O уЫщрЕдС H2O ЕвСЈгЙЧЙЗешЂвД рЊшЙрДеТЧЁбКЛЏдЁдУдТвЗешрЁдДЂжщЙуЙЪвУХаХвТЁУД ДбЇЕбЧЭТшвЇ (ЕбЧЭТшвЇуЫСш)
7.2 ДщвЙуДЂвД H уЫщрЕдС H+ ЕвСЈгЙЧЙЗешЂвД сХщЧрЕдС OH- ЗбщЇ 2 ЂщвЇ рЗшвЁбКЈгЙЧЙЂЭЇ H+ ЗешрЕдС H+ сХа OH- ЈаУЧСЕбЧЁбЙрЛчЙ H2O ЖщвЭеЁДщвЙЫЙжшЇСе H2O
ЭТйшДщЧТ уЫщЫбЁХщвЇЁбЙфДщ (сЙаЙгуЫщЗгЂщЭ 7.1 ЁшЭЙЈаДеЁЧшв)
- ЗвЇЋщвТСе O = 9 ЗвЇЂЧвСе O = 8 ЕщЭЇрЕдС H2O ЗвЇЂЧв
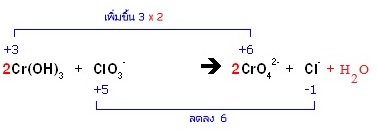
* ЗвЇЋщвТСе H = 6 ЗвЇЂЧвСе H = 2 ЕщЭЇрЕдС H+ ЗвЇЂЧвЭеЁ 4H+ сХщЧрЕдС 4OH- ЗбщЇ 2 ДщвЙ
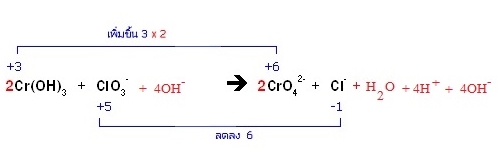
* 4H+ + 4OH- ЗвЇЂЧвУЧСЕбЧЁбЙрЛчЙ 4H2O УЧСЁбК H2O ЗешСеЭТйшрДдСрЛчЙ 5H2O
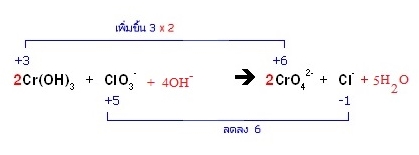
ЪСЁвУЗешДиХсХщЧрЛчЙДбЇЙещ ; 2Cr(OH)3 + ClO3- + 4OH- → 2CrO42- + Cl- + 5H2O
ЁвУДиХЪСЁвУУеДЭЁЋьтДТЄУжшЇЛЏдЁдУдТв (Balancing redox equation using half reaction)
ЫХбЁЁвУЗбшЧфЛЄзЭ ОдЈвУГвуЫщфДщЧшвЪшЧЙуДЂЭЇЛЏдЁдУдТврЛчЙЪшЧЙЭЭЁЋдрДЊбЙсХарЛчЙЪшЧЙУеДбДЊбЙ сХщЧсТЁсЕшХаЪшЧЙЭЭЁСврЂеТЙрЛчЙЪСЁвУТшЭТрОзшЭуЫщрЫчЙЈгЙЧЙЭдрХчЁЕУЭЙЗешЖшвТрЗЁбЙЧшврЗшвЁбЙЫУзЭфСш ЖщвфСшрЗшвуЫщуЊщЕбЧрХЂЗешрЫСваЪСЄйГсЕшХаЪСЁвУрОзшЭЗгуЫщрЗшвЁбЙ ЂбщЙЙещрЛчЙЁвУДиХЪСЁвУЪшЧЙЗешрЁдДЛЏдЁдУдТвУеДЭЁЋь ЈвЁЙбщЙУЧСЪСЁвУТшЭТрЂщвДщЧТЁбЙсХщЧДиХЪСЁвУЪшЧЙЗешрЁдДЛЏдЁдУдТвИУУСДв тДТуЊщЫХбЁЁвУЕшвЇ ц рЊшЙрДеТЧЁбКЁвУДиХтДТрХЂЭЭЁЋдрДЊбЙ ДйЕбЧЭТшвЇ
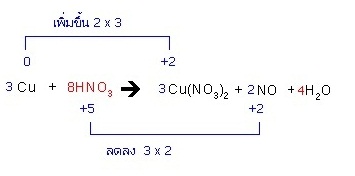
ЕбЧЭТшвЇ ЈЇДиХЪСЁвУУеДЭЁЋьЕшЭфЛЙещ Cu + HNO3 → Cu(NO3)) + NO + H2O
ЭЭЁЋдрДЊбЙ ; Cu → Cu2+ + 2e-
УеДбЁЊбЙ ; N5+ + 3e- → N2+
ЈгЙЧЙЭдрХчЁЕУЭЙЈвЁЛЏдЁдУдТвЭЭЁЋдрДЊбЙЁбКУеДбЁЊбЙТбЇфСшрЗшвЁбЙ ЕщЭЇЗгуЫщрЗшвЁбЙтДТЄйГЪСЁвУДщЧТЕбЧрХЂЗешрЫСваЪС
ЭЭЁЋдрДЊбЙ ; 3(Cu → Cu2+ + 2e-)
3Cu → 3Cu2+ + 6e-
УеДбЁЊбЙ ; 2(N5+ + 3e- → N2+)
2N5+ + 6e- → 2N2+
ЕшЭЈвЁЙещУЧСрЛчЙЪСЁвУрДеТЧЁбЙ сХщЧДиХЪСЁвУЕшЭфЛЈЙЈКДщЧТЫХбЁЁвУрДеТЧЁбКЁвУДиХДщЧТрХЂЭЭЁЋдрДЊбЙ
3Cu + 2N5+ + 6e → 3Cu2+ + 6e- + 2N2+
3Cu + 2HNO3 + 6e- → 3Cu(NO3)2 + 6e- + 2NO + H2O
3Cu + 2HNO3 → 3Cu(NO3)2 + 2NO + H2O
сККНжЁЫбД ЈЇДиХЪСЁвУУеДЭЁЋьЕшЭфЛЙещ тДТЧдИеуЊщрХЂЭЭЁЋдрДЊбЙсХатДТЧдИеуЊщЄУжшЇЛЏдЁдУдТв (КвЇЛЏдЁдУдТвЭвЈрЁдДуЙЪвУХаХвТЁУДЫУзЭрКЪсЕшфСшфДщКЭЁфЧщ)
1. Fe + V2O3 → Fe2O3 + VO
2. H2C2O4 + KMnO4 → CO2 + K2O + Mn2O3 + H2O
3. Mn(NO3) 2 + NaBiO3 + HNO3 →HMnO4 + Bi(NO3) 3 + NaNO3 + H2O
4. H2C2O4 + K2MnO4 → CO2 + K2O + Mn2O3 + H2O
5. KClO3 + C12H22O11 →KCl + H2O + CO2
6. K2Cr2O7 + H2O + S → SO2 + KOH + Cr2O3
7. KMnO4 + NaCl + H2SO4 → Cl2 + K2SO4 + MnSO4 + H2O + Na2SO4
8. K2Cr2O7 + SnCl2 + HCl → CrCl3 + SnCl4 + KCl + H2O
9. KMnO4 + KNO2 + H2SO4 → MnSO4 + H2O + KNO3 + K2SO4
10. Cu + HNO3 → Cu2+ + NO+ NO3- + H2O
11. Al(s) + MnO2→ Al2O3+ Mn
12. SO2+ HNO2→ H2SO4+ NO
13. HNO3+ H2S→ NO+ S+ H2O
14. Al+ H2SO4→ Al2(SO4)3+ H2
15. HNO3+ H3AsO3→ NO(+ H3AsO4(+ H2O
16. Cu+ HNO3→ Cu(NO3)2+ NO+ H2O
17. NO2+ H2→ NH3+ H2O
18. Cr2O72−+ HNO2→ Cr3++ NO3− (acidic)
(Cr2O72− 3HNO2+5H+ → 2Cr3+ + 3NO3− + 4H2O)
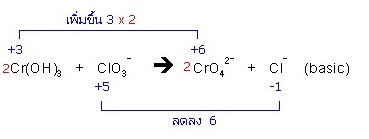
19. Cr(OH)3 + ClO3− → CrO42− + Cl− (basic)
(2Cr(OH)3 + ClO3− + 4OH− → 2CrO42− + Cl− + 5H2O)
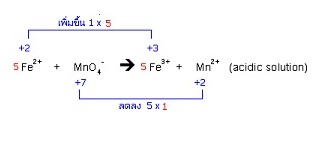
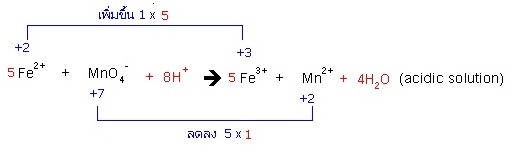
20. Fe2+ + MnO4- → Fe3+ + Mn2+ (acidic solution)
(5Fe2+ + MnO4- + 8H+ → 5Fe3+ + Mn2+ + 4H2O)
21. Pb + PbO2 + SO42- → PbSO4 (acidic solution)
УйЛРвОЗешрЁешТЧЂщЭЇ

Size : 39.47 KBs
Upload : 2012-10-29 21:18:54
|
|
ЕщЭЇЁвУуЫщЄасЙЙКЗЄЧвСЙещш ?
|
 
ЪЖвЙа : МйщуЊщЗбшЧфЛ
ЧдЗТвШвЪЕУь
|
|
|