ЂЭЇсЂчЇ ЂЭЇрЫХЧ сЁъЪ (ЕЭЙЗеш 5) ЁЎЂЭЇКЭТХь
ЁЎЂЭЇсЁъЪ
СеЙбЁЧдЗТвШвЪЕУьЈгЙЧЙСвЁЗешЪЙуЈсХаШжЁЩвЪСКбЕдЂЭЇсЁъЪ тДТрЛчЙЁвУШжЁЩврЁешТЧЁбКЄЧвСЪбСОбЙИьУаЫЧшвЇ ЈгЙЧЙтСХ ЭиГЫРйСд ЄЧвСДбЙ сХаЛУдСвЕУ ЂЭЇсЁъЪуЙУйЛсККЕшвЇ ц ЁгЫЙДуЫщ
n = ЈгЙЧЙтСХЂЭЇсЁъЪ
T = ЭиГЫРйСдЂЭЇсЁъЪ (рЄХЧдЙ ,K)
P = ЄЧвСДбЙЂЭЇсЁъЪ
V = ЛУдСвЕУЂЭЇсЁъЪ
ЁЎЂЭЇКЭТХь (Boyle,s law) (Є.Ш. 1662 О.Ш.2205)
Є.Ш. 1662 (О.Ш. 2205 ЪСбТЁУиЇШУеЭТиИТв) УЭрКдУьЕ КЭТХь (Robert Boyle) ЙбЁрЄСеЊвЧЭбЇЁФЩ ШжЁЩвЄЧвСЪбСОбЙИьУаЫЧшвЇЛУдСвЕУЁбКЄЧвСДбЙЂЭЇсЁъЪЗешСеЈгЙЧЙтСХ (ЫУзЭСЧХ) сХаЭиГЫРйСдЄЇЗеш фДщМХЁвУЗДХЭЇрУеТЁЧшв “ЁЎЂЭЇКЭТХь” ДбЇЙещ рСзшЭЈгЙЧЙтСХ (ЫУзЭСЧХ )сХаЭиГЫРйСдЂЭЇсЁъЪЄЇЗеш ЛУдСвЕУЂЭЇсЁъЪЈасЛУМЁМбЙ (varies Inversely) ЁбКЄЧвСДбЙ сХаМХЄйГУаЫЧшвЇЛУдСвЕУЁбКЄЧвСДбЙрЛчЙЄшвЄЇЗеш ; PV = k
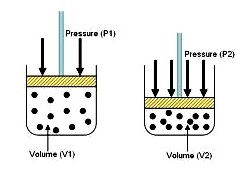
ЕбЧЭТшвЇМХЁвУЗДХЭЇ (сЁъЪСеЈгЙЧЙтСХсХаЭиГЫРйСдЄЇЗеш)
|
ЁвУЗДХЭЇ
ЄУбщЇЗеш
|
ЛУдСвЕУ
(V , dm3)
|
ЄЧвСДбЙ
(P , mmHg)
|
PV
(mmHg. cm3)
|
|
1
|
5.00
|
760
|
3.80 x 103
|
|
2
|
10.00
|
380
|
3.80 x 103
|
|
3
|
15.00
|
253
|
3.80 x 103
|
|
4
|
20.00
|
191
|
3.82 x 103
|
|
5
|
25.00
|
151
|
3.78 x 103
|
|
6
|
30.00
|
127
|
3.81 x 103
|
ЈвЁЕбЧЭТшвЇМХЁвУЗДХЭЇЈарЫчЙфДщЧшвЛУдСвЕУ (V) ЁбКЄЧвСДбЙ (P) ЂЭЇсЁъЪЈарЛХешТЙсЛХЇфЛуЙЗвЇЕУЇЁбЙЂщвС рУеТЁЧшвсЛУМЁМбЙЁбЙ ( varies Inversely ) сЕш МХЄйГУаЫЧшвЇЄЧвСДбЙЁбКЛУдСвЕУ (PV) рЛчЙЄшвЄЇЗеш сХарСзшЭрЂеТЙЁУвПсЪДЇЄЧвСЪбСОбЙИьУаЫЧшвЇЄЧвСДбЙ ( P ) ЁбКЛУдСвЕУ ( V ) ЂЭЇсЁъЪЈарЛчЙДбЇЙещ
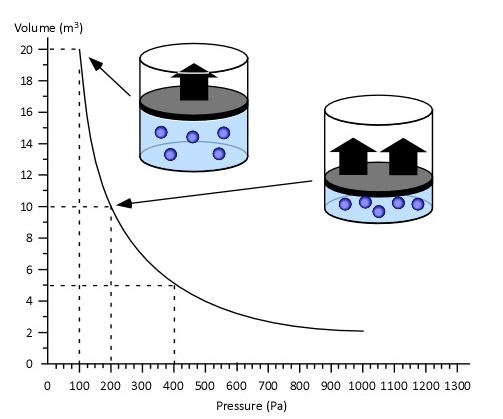
ЪбЇрЁЕЁУвПсЪДЇЄЧвСЪбСОбЙИьУаЫЧшвЇЛУдСвЕУЁбКЄЧвСДбЙ ( V ЁбК P ) ЈафСшрЛчЙрЪщЙЕУЇ сЕшЖщврЂеТЙЁУвПсЪДЇЄЧвСЪбСОбЙИьУаЫЧшвЇ V ЁбК ЫУзЭ P ЁбК ЈафДщЁУвПЗешрЛчЙрЪщЙЕУЇ
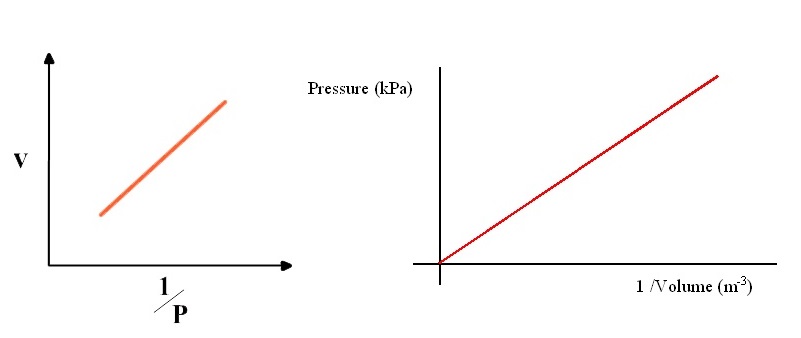
ЁвУЄгЙЧГЪСКбЕдЂЭЇсЁъЪЕвСЁЏЂЭЇКЭТХь
- ЛУдСвЕУсЛУМЁМбЙЁбКЄЧвСДбЙ рЂеТЙЧшв
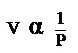
- МХЄйГУаЫЧшвЇЄЧвСДбЙЁбКЛУдСвЕУрЛчЙЄшвЄЇЗеш рЂеТЙЧшв PV = k
рЙзшЭЇЈвЁСеЁвУЗДХЭЇЋщгЫХвТ ц ЄУбщЇ ЈгЙЧЙ PV ЈаСеЫХвТЄУбщЇДщЧТ сЕшрЛчЙЄшвЄЇЗеш рЊшЙ
P1V1 = k1 ………. (1)
P2V2 = k2 .……….(2)
PnVn = kn ………. (n)
ЪСЁвУрОзшЭЁвУЄдДЄгЙЧГДщЧТЁЎЂЭЇКЭТХьЄзЭ P1V1 = P2V2 … = PnVn = k
рЂеТЙЪбщЙ ц Чшв P1V1 = P2V2
* P1 ЁбК P2 ЕщЭЇрЛчЙЫЙшЧТрДеТЧЁбЙ
* V1 ЁбК V2 ЕщЭЇрЛчЙЫЙшЧТрДеТЧЁбЙ
ЕбЧЭТшвЇЗеш 1 сЁъЪЊЙдДЫЙжшЇСеСЧХ 15 ЁУбС СеЛУдСвЕУ 10 dm3 ЗешЄЧвСДбЙ 150 mmHg рСзшЭЭиГЫРйСдЄЇЗеш Жщв
рЛХешТЙЄЧвСДбЙрЛчЙ 50 mmHg сЁъЪЈаСеЛУдСвЕУрЗшвуД
ЧдИеЗг ЁшЭЙЭзшЙуЫщЄдДрЭвфЧщЧшвЪСКбЕдЂЭЇсЁъЪЕвСЁЎЂЭЇКЭТХь рЛчЙЁвУрЛУеТКрОзшЭЫвЄЧвСЪбСОбЙИьУаЫЧшвЇЛУдСвЕУ (V) ЁбКЄЧвСДбЙ (P) ЂЭЇсЁъЪЗешСеЈгЙЧЙтСХ (n) сХаЭиГЫРйСд (T) ЄЇЗеш ЖщвтЈЗТьЁгЫЙДЂщЭСйХСвуЫщЭТшвЇрОеТЇОЭ уЫщуЊщЂщЭСйХЕвСЗештЈЗТьЁгЫЙД сЕшЖщвСеЂщЭСйХфСшрОеТЇОЭуЫщрЛУеТКрЗеТКЁбКРвЧа STP ЪгЫУбКЕбЧЭТшвЇЙещтЈЗТьуЫщЂщЭСйХСвЄУКЗбщЇ P1 P2 сХа V1 сХщЧЖвСЄшв V2
P1 = 150 mmHg
P2 = 50 mmHg
V1 = 10 ХдЕУ
V2 = ?
ЈвЁЁЎЂЭЇКЭТХь P1V1 = P2V2
150 x 10 = 50 x V2
= 30 ХдЕУ
ЕбЧЭТшвЇЗеш 2 уЊщ Mg ЈгЙЧЙ 1.00 тСХ ЗгЛЏдЁдУдТвЁбКЪвУХаХвТЁУД HCl ЋжшЇСвЁрЁдЙОЭ рЁдДЛЏдЁдУдТвДбЇЪСЁвУ : Mg(s) + 2HCl(aq) è MgCl2(aq) + H2(g)
ЖщвЗДХЭЇЗешЭиГЫРйСд 0 oC ЄЧвСДбЙ 0.80 atm ЈафДщ H2 Ёеш dm3
ЧдИеЗг ЁУГеЙещрСзшЭОдЈвУГвЪдшЇЗештЈЗТьЁгЫЙДСвуЫщЈаСеДбЇЙещ
1. ЁгЫЙДЈгЙЧЙтСХЂЭЇ Mg ЗгуЫщЫвЈгЙЧЙтСХЂЭЇ H2 фДщ
ЈвЁЪСЁвУ ; ЈгЙЧЙтСХЂЭЇ H2 ЗешфДщ = ЈгЙЧЙтСХЂЭЇ Mg ЗешуЊщ
ЈгЙЧЙтСХ (n)ЂЭЇ H2 = 1.00 тСХ
2. ЁгЫЙДЭиГЫРйСд (T) = 0 oC
3. ЁгЫЙДЄЧвСДбЙ (P) = 0.8 atm
ЂщЭСйХЕвСЗештЈЗТьЁгЫЙДСвЙещЭиГЫРйСдсХаЄЧвСДбЙСерОеТЇЊЙдДХа 1 Єшв сЕшЭиГЫРйСдЗешЁгЫЙДЄзЭ 0 oC ЋжшЇрЛчЙЭиГЫРйСдЂЭЇРвЧа STP ЖщвОКЄгЖвСЗгЙЭЇЙещуЫщЙгРвЧаЗештЈЗТьЁгЫЙДфЛрЛУеТКрЗеТКЁбКРвЧа STP ЫУзЭуЙЭеЁЁУГеЫЙжшЇ ЁгЫЙДЄЧвСДбЙСвуЫщЄшврДеТЧсХа = 1 atm ЋжшЇрЛчЙЄЧвСДбЙЗешРвЧа STP рЊшЙЁбЙ ЈжЇЄдДЄгЙЧГфДщтДТЙгфЛрЛУеТКрЗеТКЁбКРвЧа STP
* сЕшЖщвЁгЫЙДЭиГЫРйСдЫУзЭЄЧвСДбЙСвЭТшвЇХаЄшврДеТЧ сЕшфСшуЊш 0 oC фСшуЊш 1 atm ЈаЄгЙЧГтДТуЊщЁЎЂЭЇКЭТХьфСшфДщ
ЧдИеЄдДрЛчЙДбЇЙещ
ЗешРвЧа STP (уЫщрЛчЙРвЧаЗеш 1 )
n = 1 mol
T = 0 oC
P1 = 1 atm
V1 = 22.4 dm3
ЗешРвЧаЕвСтЈЗТьЁгЫЙД (уЫщрЛчЙРвЧаЗеш 2)
n = 1 mol
T = 0 oC
P2 = 0.8 atm
V2 = ?
ЁЎЂЭЇКЭТХь
P1V1 = P2V2
1.00 x 22.4 = 0.80 x V2
= 28.00 dm3 ЕЭК
ЄгЖвС V1 = 22.4 dm3 сХа V2 = 28.00 dm3 ЗбщЇ 2 ЁУГеЙещсЁъЪСеЈгЙЧЙтСрЗшвЁбЙЫУзЭфСш
ЫСвТрЫЕи ЫЙшЧТЄЧвСДбЙКУУТвЁвШЫЙшЧТЭзшЙ ц ЗешЄЧУЗУвКфДщсЁш
** ЛвЪЄвХ (Pa) 1 ЛвЪЄвХСеЄшврЗшвЁбК 9.8692×10−6 atm
** 1 atm рЗшвЁбК 101.325 kPa (ЁдтХЛвЪЄвХ)
** ЛЭЙДь/ЕвУвЇЙдщЧ (pound per square inch, Psi) ; 14.7 ЛЭЙДь ЕшЭЕвУвЇЙдщЧ = 1 КУУТвЁвШ
** 1 atm рЗшвЁбК 1 КвУь
(ЄХдщЁ ЊСЁвУЗДХЭЇЂЭЇКЭТХь)
сККНжЁЫбД
1. сЁъЪЊЙдДЫЙжшЇКУУЈиуЙЖбЇрЫХчЁЗешСеЛУдСвЕУ 20 ХдЕУ СеЄЧвСДбЙ x atm ЖщвЖшвТсЁъЪЈгЙЧЙЙещфЛуЪшЖбЇ
ЪивЁвШЭеЁуКЫЙжшЇЋжшЇСеЛУдСвЕУ 5 ХдЕУсХаСеЭиГЫРйСдрЗшврДдС ОКЧшвСеЄЧвСДбЙ 18 atm ЈЇЫвЄЧвС
ДбЙЂЭЇсЁъЪуЙЖбЇуКрДдС
1. 2 atm 2. 4.5 atm 3. 12 at 4. 25.5 atm
2. сЁъЪЊЙдДЫЙжшЇСеЛУдСвЕУ 500 cm3 ЗешЄЧвСДбЙ 1 КУУТвЁвШ ЭиГЫРйСд 27 oC рСзшЭХДЛУдСвЕУЂЭЇсЁъЪХЇ
рЫХзЭ 100 cm3 тДТЭиГЫРйСдсХаСЧХЂЭЇсЁъЪЄЇЗеш ЧбДЄЧвСДбЙфДщ 4 КУУТвЁвШ ЈЇЄгЙЧГЫвЧшвЄЧвС
ДбЙЗешЧбДфДщСеЄЧвСЄХвДрЄХзшЭЙфЛЈвЁЄЧвСДбЙЗешрЛчЙфЛЕвСЁЎЂЭЇКЭТХьЁешрЛЭУьрЋчЙЕь
1. 20 2. 40 3. 60 4. 80
3. At constant temperature, a sample of 3.0 L of Ne gas at 2.0 atm is compress until the pressure is
3.524 atm. What is the new volume? (сЁъЪЙеЭЭЙ 3.0 ХдЕУ СеЄЧвСДбЙ 2.0 atm ЖйЁЭбДЈЙЗгуЫщЄЧвС
ДбЙрОдшСЂжщЙрЛчЙ 3.524 atm тДТЭиГЫРйСдЄЇЗеш ЛУдСвЕУЂЭЇсЁъЪрЛчЙрЗшвфУ)
4. A fix quantity of gas at a constant temperature exhibits a pressure of 737 torr and
occupied a volume of 20.5 L. Use Boyle’s law ; (сЁъЪЋжшЇСеЛУдСвГсХаЭиГЫРйСдЄЇЗеш СеЄЧвСДбЙ
737 torr СеЛУдСвЕУ 20.5 ХдЕУ ЈЇуЊщЁЎЂЭЇКЭТХь )
a. the volume the gas will occupy if the pressure is increases to 1.80 atm. (ЖщвЗгуЫщЄЧвС
ДбЙрОдшСЂжщЙрЛчЙ 1.80 atm ЛУдСвЕУЂЭЇсЁъЪЈарЛчЙрЗшвфУ)
b. the pressure of the gas if the volume is decrease to 16.0 L. (ЖщврХДЛУдСвЕУрЫХзЭ 16
ХдЕУ ЄЧвСДбЙЈарЛчЙрЗшвфУ)
5. Calculate the final pressure of each gas, assuming that the temperature remaining
constant at 25 oC. (ЈЇЄгЙЧГЫвЄЧвСДбЙЂЭЇсЁъЪсЕшХаЊЙдДЕшЭфЛЙещ ЋжшЇСеЭиГЫРйСд 25 oC ЄЇЗеш)
a. 2.02 cm3 of CO at 724 torr expands to 25.00 mL. (сЁъЪ CO 2.02 cm3 СеЄЧвСДбЙ 724
torr ЗгуЫщЛУдСвЕУрОдшСЂжщЙрЛчЙ 25.00 mL)
b. 57.66 mL of H2 at 2.00 atm is compress to 5.11 mL. ( сЁъЪ H2 57.66 mL СеЄЧвСДбЙ 2.00
atm ЭбДЈЙЛУдСвЕУХДХЇрЫХзЭ 5.11 mL)
c. 1200 L of He at 1.00 atm expands to 5200 L. ( сЁъЪ He 1200 L СеЄЧвСДбЙ 1.00 atm ЂТвТ
ЛУдСвЕУрЛчЙ 5200 L.)
6. Calculate the final volume for each of these gases. The temperature remains constant at
25 oC in all cases. (ЈЇЄгЙЧГЫвЛУдСвЕУЂЭЇсЁъЪсЕшХаЊЙдДЕшЭфЛЙещ ЋжшЇСеЭиГЫРйСд 25 oC ЄЇЗеш)
a. 2.00 x 103 L of NH3 at 1.00 atm in place under under a pressure of 500 torr. (сЁъЪ
сЭСтСрЙеТ 2.00 x 103 L СеЄЧвСДбЙ 1.00 atm ЗгуЫщЄЧвСДбЙХДХЇрЫХзЭ 500 torr)
b. 2.555 atm of pressure is applied to 20.56 mL of H2 at 1.00 atm.(сЁъЪ H2 ЈгЙЧЙ 20.56
mL СеЄЧвСДбЙ 1.00 atm ЖщвСеЄЧвСДбЙ 2.555 atm СеЛУдСвЕУрЗшвфУ)
c. 50.0 atm of pressure is applied to 7.70 x 103 L of He at 0.977 atm. (сЁъЪ He СеЛУдСвЄУ
7.70 x 103 L ЗешЄЧвСДбЙ 0.977 atm ЖщвСеЄЧвСДбЙ 50.0 atm СеЛУдСвЕУрЗшвфУ )
8. A gas bubble has a volume of 0.650 mL at the bottom of a lake at 81 feet, where the total pressure
is 3.46 atm. What is the volume of the bubble when it reaches the surface of the lake, where the
pressure is 1.00 atm? Assume that the temperature is constant. (ans.e) ; (ПЭЇЁъвШЂГаЭТйшЁщЙ
ЗарХЪвКХжЁ 81 ПиЕ СеЛУдСвЕУ 0.650 mL ЂГаЙбщЙСеЄЧвСДбЙ 3.46 atm рСзшЭПЭЇсЁъЪХЭТЕбЧЂжщЙСвЖжЇМдЧ
ЙщгЋжшЇСеЄЧвСДбЙ 1.00 atm ПЭЇсЁъЪЈаСеЛУдСвЕУрЗшвфУ)
a) 1.20 mL b) 0.188 mL c) 1.90 mL d) 0.122 mL e) 2.25 mL
9. A 6.5 L sample of nitrogen at 25oC and 1.5 atm is allowed to expand to 13.0 L. The temperature remains constant. What is the final pressure (atm)? (ans.e) ; (ЗешЭиГЫРйСд25oC ЄЧвСДбЙ 1.5 atm сЁъЪфЙтЕУрЈЙЈгЙЧЙЫЙжшЇСеЛУдСвЕУ 6.5 L ЖщврОдшСЛУдСвЕУЂжщЙрЛчЙ 13.0 L тДТЭиГЫРйСдЄЇЗеш ЄЧвСДбЙЂЭЇсЁъЪЈарЛчЙЁеш atm)
a) 0.380 b) 0.12 c) 3.0 d) 0.063 e) 0.75
10. The volume of one cylinder in an automobile is 0.44 L. The cylinder is filled with a gasoline and air mixture at 1.0 atm and then is compressed to 0.073 L prior to ignition. What pressure must be applied to produce this compression? (ans.d) ; (ЁУаКЭЁЪйКЂЭЇрЄУзшЭЇТЙЕьСеЛУдСвЕУ 0.44 L СефЭЂЭЇЙщгСбЙсЁЪтЋХеЙМЪСЁбК ЭвЁвШКУУЈиЭТйшСеЄЧвСДбЙ 1 atm рСзшЭрЁдДЁвУЭбДЈЙЛУдСвЕУХДХЇрЫХзЭ 0.073 L ЄЧвСДбЙЈарЛчЙрЗшвфУ)
a) 4.4 atm b) 3.6 atm c) 3.1 atm d) 6.0 atm e) 7.3 atm
11. An adult human breathes 0.50 L of air at 1.0 atm with each breath. If a 50 L air tank at 200 atm is available, how many breaths will the tank provide? (ans.c) ; (ЛЭДЂЭЇМйщуЫшЈиЭвЁвШфДщ 0.5 L ЗешЄЧвСДбЙ 1 atm ЕшЭЁвУЫвТуЈ 1 ЄУбщЇ ЖщвЫвТуЈтДТуЊщЭвЁвШЈвЁЖбЇЂЙвД 50 L ЄЧвСДбЙ 200 atm ЈаЫвТуЈфДщЁешЄУбщЇ)
a) 5.0 x 104 b) 4.0 x 104 c) 2.0 x 104 d) 1.0 x 104 e) 5.0 x 103
УйЛРвОЗешрЁешТЧЂщЭЇ

Size : 45.27 KBs
Upload : 2014-02-13 05:27:50
|
|
ЕщЭЇЁвУуЫщЄасЙЙКЗЄЧвСЙещш ?
|
 
ЪЖвЙа : МйщуЊщЗбшЧфЛ
ЧдЗТвШвЪЕУь
|
|
|