ЛУдСвГЪвУЪбСОбЙИь ЕЭЙЗеш 5 ЄЧвСрЂщСЂщЙ тСХ/ХдЕУ
4. тСХ/ХдЕУ ,mol/l ЫУзЭ тСХ/ХйЁКвШЁьрДЋдрСЕУ, mol/dm3ЫУзЭ тСХвУдЕе , molarity ЫУзЭ тСХвУь ,molar, M
ЄЧвСрЂщСЂщЙЊЙдДЙещСеЁвУЙгфЛуЊщЭТшвЇЁЧщвЇЂЧвЇ СеХбЁЩГарЛчЙЁвУКЭЁЈгЙЧЙтСХЂЭЇЕбЧХаХвТ ЗешСеЭТйшуЙЪвУХаХвТ 1.0 ХдЕУ ЫУзЭ 1.0 dm3 ЫУзЭ 1,000 cm3 рЊшЙ уЊщ C6H12O6 ЈгЙЧЙ 0.10 тСХ (ЫЙбЁ 18.0 ЁУбС) ЗгуЫщрЛчЙЪвУХаХвТ 1.0 ХдЕУ ЪвУХаХвТЗешфДщЈаСеЄЧвСрЂщСЂщЙ 0.10 тСХ/ХдЕУ ДбЇУйЛ
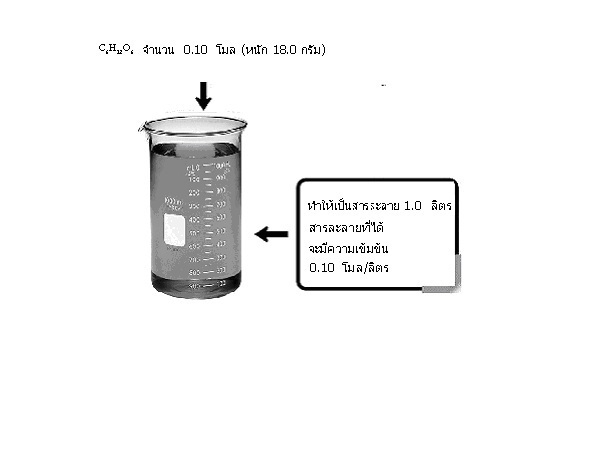
ЕбЧЭТшвЇ ЙщгЕвХЁХйтЄЪ (C6H12O6) ЫЙбЁ 18.0 ЁУбС ЗгуЫщрЛчЙЪвУХаХвТ 200 cm3 ЪвУХаХвТЗешфДщЈаСеЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ
ЧдИеЗг ЙгЙЧЙтСХЂЭЇ C6H12O6 ; n = W/M =18/C6H12O6 = 18/180 = 0.10 mol
ЪвУХаХвТ 200 cm3 Се C6H12O6 ХаХвТЭТйш 0.10 mol
ЪвУХаХвТ 1,000 cm3 Се C6H12O6 ХаХвТЭТйш = .050 mol
ЄЧвСрЂщСЂщЭЙЂЭЇЪвУХаХвТ = 0.50 тСХ/ХдЕУ ЕЭК
уЊщЪйЕУ ЁгЫЙДЕбЧсЛУДбЇЙещ
n = ЈгЙЧЙтСХ
V = ЛУдСвЕУЂЭЇЪвУХаХвТ (cm3)
C = ЄЧвСрЂщСЂщЙЂЭЇЪвУХаХвТ , тСХ/ХдЕУ
ЪйЕУ n = VC/1000
* Жщв V уЊщЫЙшЧТрЛчЙ dm3 ЫУзЭ L ; n = VC
** Жщв n ЄЇЗеш ; n = N/6.02 x 1023 = W/M = VC/1000 (V рЛчЙ cm3) = VC (V рЛчЙ dm3)
ЈвЁЕбЧЭТшвЇ ; n = VC/1000
0.1 = 200C/1000
C = 0.1x1000/200
= 0.50 тСХ/ХдЕУ ЕЭК
** ЖщвЄдДЈвЁ V рЛчЙ dm3
n = VC
0.1 mol = 0.2 dm3 C
C = 0.1/0.2 = 0.50 mol/dm3 ЕЭК
- ЄЧвСрЂщСЂщЙуЙЫЙшЧТтСХ/ХдЕУ ЁбКЄЧвСрЂщСЂщЙуЙЫЙшЧТУщЭТХатДТСЧХСеЄЧвСЪбСОбЙИьЁбЙ ЄзЭЖщвЗУвКЄЧвСрЂщСЂщЙуЙЫЙшЧТУщЭТХатДТСЧХОУщЭСЁбКЄЧвСЫЙвсЙшЙ ЈарЛХешТЙрЛчЙЄЧвСрЂщСЂщЙтСХ/ХдЕУ фДщ
ЕбЧЭТшвЇ ЪвУХаХвТ C6H12O6 ЄЧвСрЂщСЂщЙУщЭТХа 10 тДТСЧХ СеЄЧвСЫЙвсЙшЙ 1.10 g/cm3 ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ
ЧдИеЗг ЪвУХаХвТСеЄЧвСЫЙвсЙшЙ 1.10 g/cm3
ЪвУХаХвТ 1 cm3 ЫЙбЁ 1.10 ЁУбС
ЪвУХаХвТ 1,000 cm3 ЫЙбЁ = 1,100 ЁУбС
ЪвУХаХвТСеЄЧвСрЂщСЂщЙУщЭТХа 10 тДТСЧХ
ЪвУХаХвТ 100 ЁУбС Се C6H12O6 ХаХвТЭТйш 10 ЁУбС
ЪвУХаХвТ 1,100 ЁУбС Се C6H12O6 ХаХвТЭТйш = 110 ЁУбС
ЄдДрЛчЙЈгЙЧЙтСХЂЭЇЁХйтЄЪ ; n = W/M = 110/180
= 0.61 тСХ
ЪвУХаХвТЙещСеЄЧвСрЂщСЂщЙ 0.61 тСХ/ХдЕУ ЕЭК
- ЄЧвСрЂщСЂщЙуЙЫЙшЧТтСХ/ХдЕУ ЁбКЄЧвСрЂщСЂщЙуЙЫЙшЧТУщЭТХатДТСЧХ/ЛУдСвЕУ СеЄЧвСЪбСОбЙИьЁбЙ ЄзЭЖщвЗУвКУщЭТХатДТСЧХ/ЛУдСвЕУ ЪвСвУЖрЛХешТЙуЫщрЛчЙтСХ/ХдЕУфДщЗбЙЗе
ЕбЧЭТшвЇ ЪвУХаХвТ C6H12O6 ЄЧвСрЂщСЂщЙУщЭТХа 10 тДТСЧХ/ЛУдСвЕУ ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ
ЄЧвСрЂщСЂщЙУщЭТХа 10 тДТСЧХ/ЛУдСвЕУ
ЪвУХаХвТ 100 cm3 Се C6H12O6 ХаХвТЭТйш 10 ЁУбС
ЪвУХаХвТ 1,000 cm3 Се C6H12O6 ХаХвТЭТйш = 1,000 ЁУбС
ЄдДрЛчЙЈгЙЧЙтСХЂЭЇЁХйтЄЪ ; n = W/M = 1,000/180
= 5.56 тСХ
ЪвУХаХвТЙещСеЄЧвСрЂщСЂщЙ 5.56 тСХ/ХдЕУ ЕЭК
сККНжЁЫбД
1. уЙЪвУХаХвТ 350.00 cm3 СетЋрДеТСЄХЭфУДь ( NaCl )ХаХвТЭТйш 10.50 ЁУбС ЈаСеЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ (Na=23 Cl=35.5)
2. ЪвУХаХвТ 125.00 cm3 СеХдрЗеТСЄХЭрУЕ , LiClO4.3H2O ХаХвТЭТйш 40.70 ЁУбС ЪвУХаХвТЈаСеЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ (Li=7 Cl=35.5 O=16 H=1)
3. ЪвУХаХвТ 0.355 dm3 СесСЁЙерЋеТСтКУфСДь , MgBr2 ХаХвТЭТйш 25.00 ЁУбС ЈаСеЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ (Mg=24 Br=80)
4. ЪвУХаХвТ 185.00 cm3 СесСЇЁвЙеЪ (II) фЙрЕУЕ , Mn(NO3)2.2H2O ХаХвТЭТйш 5.66 ЁУбС ЈаСеЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ (Mn=55 N=14 O=16)
5. ЈЇЄгЙЧГЫвЄЧвСрЂщСЂщЙуЙЫЙшЧТ molarity ЂЭЇЪвУХаХвТЕшЭфЛЙещ (Li=7 O=16 S=32 Na=23 C=12 H=1)
5.1 Li2SO3 ЈгЙЧЙ 4.67 mole уЙЪвУХаХвТЗешСеЛУдСвЕУ 2.04 ХдЕУ
5.2 Li2SO3 ЈгЙЧЙ 0.629 mole уЙЪвУХаХвТЗешСеЛУдСвЕУ 1.50 ХдЕУ
5.3 Na2CO3 ЈгЙЧЙ 4.783 g уЙЪвУХаХвТЗешСеЛУдСвЕУ 10.01 ХдЕУ
5.4 (NH4)2CO3 ЈгЙЧЙ 0.897 g уЙЪвУХаХвТЗешСеЛУдСвЕУ 250 cm3
6. ЈЇЄгЙЧГЫвЈгЙЧЙтСХЂЭЇЕбЧЖйЁХаХвТуЙЪвУХаХвТЕшЭфЛЙещ (Cu=63.5 Mg=24 Pb=207)
6.1 ЪвУХаХвТ Cu(NO3) ЄЧвСрЂщСЂщЙ 22.0 M ЛУдСвЕУ 2.35 dm3
6.2 ЪвУХаХвТ MgCO3 ЄЧвСрЂщСЂщЙ 0.50 M ЛУдСвЕУ 3.00 dm3
6.3 ЪвУХаХвТ Pb(NO3)2 ЄЧвСрЂщСЂщЙ 0.415 M ЛУдСвЕУ 16.00 cm3
6.4 ЪвУХаХвТ Na2O ЄЧвСрЂщСЂщЙ 3.76 M ЛУдСвЕУ 6.20 cm3
7. ЈЇЄгЙЧГЫвСЧХ(ЁУбС)ЂЭЇЕбЧХаХвТуЙЪвУХаХвТЕшЭфЛЙещ ( K=39 Cl=35.5 Na=23 O=16 )
7.1 ЪвУХаХвТ KCl ЄЧвСрЂщСЂщЙ 1.00 тСХшвУь ЛУдСвЕУ 0.500 dm3
7.2 ЪвУХаХвТ Na2O ЄЧвСрЂщСЂщЙ 3.76 тСХшвУь ЛУдСвЕУ 6.02 dm3
8. ЈЇЄгЙЧГЫвЈгЙЧЙтСХсХаСЧХ (ЁУбС) ЂЭЇ NaCl ЗешСеЭТйшуЙЪвУХаХвТ ЋжшЇСеЄЧвСрЂщСЂщЙ 0.20 M сХаСеЛУдСвЕУ100 cm3
9. ЪвУХаХвТ NaOH рЂщСЂщЙ 0.25 M ЈгЙЧЙ 300 cm3 ЈаСе NaOH ХаХвТЭТйшЁешЁУбС (Na=23 O=16 H=1) (ЕЭК 3.00 ЁУбС)
10. ЪвУХаХвТ 575 cm3 Се NaCl ХаХвТЭТйш 9.25 ЁУбС ЈаСеЄЧвСрЂщСЂщЙЁештСХвУь (ЕЭК 0.284 M )
11. ЪвУХаХвТ NaCl ЄЧвСрЂщСЂщЙ 5.32 % тДТСЧХ/СЧХ СеЄЧвСЫЙвсЙшЙ 1.10 g/cm3 ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ
12. ЪвУХаХвТ H2SO4 рЂщСЂщЙ 10 % тДТСЧХ/СЧХ СеЄЧвСЫЙвсЙшЙ 1.07 g/cm3 ЈаСеЄЧвСрЂщСЂщЙЁештСХшвУь (H=1 O=16 S=16) (ЕЭК 1.09 )
13. ЪвУХаХвТ K2SO4 рЂщСЂщЙ 0.50 M ЈаСеЄЧвСрЂщСЂщЙУщЭТХарЗшвфУтДТСЧХ/ЛУдСвЕУ (ЕЭК 8.70)
14. ЁъвЋфЮтДУрЈЙЄХЭфУДьЫЙбЁ 1.46 ЁдтХЁУбС ЙгфЛХаХвТЙщгЈЙфДщЪвУХаХвТЁУДфЮтДУУдЁ 10 dm3 ЪвУХаХвТЁУДЙещСеЄЧвСрЂщСЂщЙрЗшвуД (Ent’23) (H=1 Cl=35.6)
1. 0.146 g/dm3 2. 14.6 % (тДТСЧХ/СЧХ) 3. 4 mol/dm3 4. .0.4 mol/dm3
15. ЙщгЪщСЪвТЊйЊЙдДЫЙжшЇ СеЄЧвСЫЙвЙсЙшЙ 1.13 g/cm3 УаКиЧшвСеЁУДсЭЋеЕдЁХаХвТЭТйшУщЭТХа 8 тДТЙщгЫЙбЁЙщгЪщСЪвТЊйЙещЈаСеЄЧвСрЂщСЂщЙЄдДрЛчЙЁеш mol/dm3 (ENT’43)
1. 0.13 2. 1.33 3. 1.51 4. 7.1
16. МшвЙЁъвЋ A ХЇуЙЙщгЈгЙЧЙЫЙжшЇ фДщЪвУХаХвТЁУД B ЗешСеЄЧвСрЂщСЂщЙУщЭТХа 30 тДТСЧХ сХаСеЄЧвСЫЙвсЙшЙ 1.10 ЁУбСЕшЭХйЁКвШЁьрЋЙЕдрСЕУ ЖщвСЧХтСрХЁиХЂЭЇ B = 66 ЪвУХаХвТЁУД B СеЄЧвСрЂщСЂщЙЁештСХЕшЭХйЁКвШЁьрДЋдрСЕУ (ENT’37)
1. 5 2. 10 3. 20 4. 25
17. ЂЭЇрЫХЧЊЙдДЫЙжшЇСеЪйЕУрЛчЙ A3B СеЄЧвСЖшЧЇЈгрОва 1.50 (СЧХЭаЕЭСЂЭЇA=33,B=21) рСзшЭЙгA3B 20 cm3 МЪСЁбКЙщгуЫщСеЛУдСвЕУЪиДЗщвТрЗшвЁбК 500 cm3 ЪвУХаХвТЗешфДщЈаСеЄЧвСрЂщСЂщЙЁеш mol/dm3 (ENT’26)
1. 2.00 2. 1.50 3. 1.00 4. 0.50
18. рСзшЭрЕдСМХжЁ AgNO3 1.70 ЁУбСХЇуЙЪвУХаХвТ AgNO3 0.10 mol/dm3 250 cm3 сХщЧЄЙЈЙМХжЁХаХвТЫСДЪвУХаХвТ AgNO3 уЫСшЗешфДщЈаСеЄЧвСрЂщСЂщЙЁеш mol/dm3 ЪССЕдЧшвЛУдСвЕУЂЭЇЪвУХаХвТЄЇЗеш (ENT’26) (Ag=108 O=16 N=14)
1. 0.11 2. 0.14 3. 0.28 4. 0.44
19. (PAT.2 Е.Є.51) СеЪвУХаХвТ NaOH 500 cm3 фСшЗУвКЄЧвСрЂщСЂщЙ рСзшЭсКшЇЪвУХаХвТ NaOH ЙещСв 100 cm3 рЕдСЙщгХЇфЛ 300 cm3 ЛУвЁЏЧшвфДщЪвУХаХвТрЂщСЂщЙ 0.10 тСХ/ХдЕУ ЖщвЙгЪвУХаХвТ NaOH ЗешрЫХзЭЗбщЇЫСДЋжшЇфСшЗУвКЄЧвСрЂщСЂщЙЙещ СврЕдСЙщгХЇфЛ 400 cm3 ЈафДщЪвУХаХвТрЂщСЂщЙЁештСХ/ХдЕУ
1. 0.20 2. 0.30 3. 0.40 4. 0.50
20. Cow's milk contains 4.5 g of lactose (C12H22O11) per 0.100 L of milk. What is the molarity of lactose?
(Atomic weights: C = 12.01, H = 1.008, O = 16.00). (Ans.a); (ЖщвуЙЙщгЙСЈгЙЧЙ 0.100 ХдЕУ СесХЄтЕЪХаХвТЭТйш 4.5 ЁУбС ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ)
a) 0.13 b) 0.16 c) 0.045 d) 0.415 e) 1.3
21. Gatorade Thirst Quencher contains 0.14 g of Cl- in a 250 mL glass. What is the molarity of Cl-?
(Atomic weight: Cl = 35.45). (Ans.a); (рЄУзшЭЇДзшСсЁщЁУаЫвТЙщг 250 mL Се Cl- ХаХвТЭТйш 0.14 g ЄЧвСрЂщСЂщЙЂЭЇ Cl- рЛчЙЁештСХ/ХдЕУ)
a) 0.016 b) 0.32 c) 0.16 d) 0.56 e) 0.032
22. There are 10.0 g of calcium as Ca2+ in 1.0 L of milk. What is the molarity of calcium ions in milk?
(Atomic weight: Ca = 40.08). (Ans.a); (ЙщгЙС 1.0 L Се Ca2+ ХаХвТЭТйш 10.0 g ЄЧвСрЂщСЂщЙЂЭЇ Ca2+ рЛчЙЁештСХ/ХдЕУ)
a) 0.25 b) 0.025 c) 0.50 d) 0.010 e) 0.10
23. The density of a 36.0% by weight aqueous solution of (NH4)2SO4 is 1.2077 g/cm3. What is the molarity of the compound? (Atomic weights: N = 14.01, S = 32.06, O = 16.00, H = 1.008). (Ans.a); (ЪвУХаХвТ (NH4)2SO4 СеЄЧвСрЂщСЂщЙ 36.0% тДТСЧХ СеЄЧвСЫЙвсЙшЙ 1.2077 g/cm3 ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ)
a) 3.29 b) 3.82 c) 3.60 d) 4.03 e) 4.24
24. The density of a 64.0% by weight aqueous solution of glycerol (C3H8O3) is 1.1663 g/cm3. What is the molarity of the compound? (Atomic weights: C = 12.01, H = 1.008, O = 16.00). (Ans.a); (ЪвУХаХвТ glycerol (C3H8O3) СеЄЧвСрЂщСЂщЙ 64.0% тДТСЧХ СеЄЧвСЫЙвсЙшЙ 1.1663 g/cm3 ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ)
a) 8.11 b) 8.62 c) 7.51 d) 8.41 e) 7.82
25. What is the molarity of HI in a solution that is 47.0% HI and has a density equal to 1.50 g/mL?
(Atomic weights: H = 1.008, I = 126.9). (Ans.a); (ЪвУХаХвТ HI ЄЧвСрЂщСЂщЙ 47.0% СеЄЧвСЫЙвсЙшЙ 1.50 g/mL ЄдДрЛчЙЄЧвСрЂщСЂщЙЁештСХ/ХдЕУ)
a) 5.51 b) 4.76 c) 5.85 d) 5.22 e) 5.00
26. Determine the number of moles of solute present in 275 mL of 0.5151 M KClO4.
(Atomic weights: Cl = 35.45, O = 16.00, K = 39.1). (Ans.c); (ЪвУХаХвТ KClO4. ЄЧвСрЂщСЂщЙ 0.5151 M ЈгЙЧЙ 275 mL Се KClO4 ХаХвТЭТйшЁештСХ)
a) 0.112 b) 0.189 c) 0.142 d) 0.0922 e) 0.212
27. Determine the number of moles of solute present in 455 mL of 3.75 M HCl solution.
(Atomic weights: Cl = 35.45, H = 1.008). (Ans.c); (ЪвУХаХвТ HCl ЄЧвСрЂщСЂщЙ 3.75 M ЈгЙЧЙ 455 mL Се HCl ХаХвТЭТйшЁештСХ)
a) 1.23 b) 1.56 c) 1.71 d) 1.98 e) 1.89
28. How many moles of glucose are contained in 500.0 mL of 0.30 M glucose, C6H12O6, used in intravenous injection? (Atomic weights: C = 12.01, H = 1.008, O = 16.00). (Ans.c); (ЪвУХаХвТЁХйтЄЪЪгЫУбКЉеДрЂщвЗвЇрЪщЙрХзЭДДг СеЄЧвСрЂщСЂщЙЂЭЇ C6H12O6 0.30 M ЭТвЁЗУвКЧшвуЙЪвУХаХвТ 500.0 mL СеЁХйтЄЪХаХвТЭТйшЁештСХ)
a) 0.60 b) 0.015 c) 0.15 d) 1.5 e) 0.060
29. How many grams of NaCN are in 100.0 mL of 3.8 x 10-5 M NaCN? (Atomic weights: Na = 22.99, N = 14.01, C = 12.01). (Ans.e); (ЪвУХаХвТ NaCN ЄЧвСрЂщСЂщЙ 3.8 x 10-5 M ЭТвЁЗУвКЧшвуЙЪвУХаХвТ 100.0 mL ЈаСе NaCN ХаХвТЭТйшЁешЁУбС)
a) 3.8 x 10-5 b) 1.9 x 10-5 c) 2.6 x 10-6 d) 3.8 x 10-4 e) 1.9 x 10-4
30. How many grams of glucose are contained in 500.0 mL of 0.30 M glucose, C6H12O6, used in intravenous injection? (Atomic weights: C = 12.01, H = 1.008, O = 16.00). (ans.e) ; (ЪвУХаХвТЙщгЕвХЁХйтЄЪЗешуЊщЉеДрЂщврЪщЙрХзЭДДг СеЄЧвСрЂщСЂщЙЂЭЇ C6H12O6 0.30 M ЭТвЁЗУвКЧшвуЙЪвУХаХвТ 500.0 mL ЈаСеЁХйтЄЪХаХвТЭТйшЁешЁУбС)
a) 2.7 b) 1.5 c) 0.15 d) 0.27 e) 27
31. The lowest limit of MgSO4 that can be detected by taste in drinking water is 0.400 g per liter. How many moles of MgSO4 is this per liter? (Atomic weights: Mg = 24.30, O = 16.00, S = 32.06). (Ans.e) ; (СвЕУАвЙЂЭЇЙщгДзшСЭЙивЕуЫщСе MgSO4 фДщ 0.400 ЁУбС/ХдЕУ ЭТвЁЗУвКЧшвЄдДрЛчЙЁештСХ/ХдЕУ)
a) 3.32 x 10-4 b) 3.01 x 10-6 c) 3.01 x 10-4 d) 3.32 x 10-2 e) 3.32 x 10-3
32. ЪвУХаХвТ C6H12O6 ЁбКЪвУХаХвТ NaCl СеЄЧвСрЂщСЂщЙ 1 тСХ/ХдЕУ рЗшвЁбЙ тДТСеЙщгрЛчЙЕбЧЗгХаХвТрЊшЙрДеТЧЁбЙ сЕшСеУйЛсККЂЭЇЁвУХаХвТсЕЁЕшвЇЁбЙЄзЭ
C6H12O6(s) C6H12O6(aq)
NaCl(s) Na+(aq) + Cl-(aq)
ЈЇрЛУеТКрЗеТКЭбЕУвЪшЧЙУаЫЧшвЇ ЈгЙЧЙтСрХЁиХЂЭЇ C6H12O6 : ЈгЙЧЙтСрХЁиХЂЭЇЙщг
сХаЭбЕУвЪшЧЙУаЫЧшвЇ ЈгЙЧЙфЭЭЭЙ Na+ + Cl- : ЈгЙЧЙтСрХЁиХЂЭЇЙщг
УйЛРвОЗешрЁешТЧЂщЭЇ

Size : 21.20 KBs
Upload : 2013-08-05 04:04:05
|
|
ЕщЭЇЁвУуЫщЄасЙЙКЗЄЧвСЙещш ?
|
 
ЪЖвЙа : МйщуЊщЗбшЧфЛ
ЧдЗТвШвЪЕУь
|
|
|